Oxidation
Table of Contents
Die Oxidation ist ein chemischer Prozess, der stattfindet, wenn Elektronen von einem Molekül, Atom oder Ion verloren gehen. Im Zusammenhang mit der Kalorimetrie wird die Oxidation oft als thermische Analyse untersucht, bei der es um das Verbrennen oder den Abbau von Substanzen geht, um Energie in Form von Wärme freizusetzen.
Dynamische Differenz-Kalorimetrie (DSC) ist eine Technik, die verwendet werden kann, um diesen Prozess zu charakterisieren, da sie den Wärmefluss misst, der mit der Oxidation einer Probe beim Erhitzen oder Abkühlen verbunden ist. Das Prinzip hinter der Messung der Oxidation mit DSC (Differentielle Scanning-Kalorimetrie) beruht auf der exothermen Natur von Oxidationsreaktionen.
Bei der DSC kann die Oxidation isotherm oder nicht-isotherm untersucht werden. Für isotherme Oxidationsstudien wird die Temperatur des DSC-Probentiegels auf einer konstanten Temperatur eingestellt und die Oxidation der Probe im Laufe der Zeit überwacht.
Der Beginn der Oxidation wird typischerweise durch das Auftreten eines exothermen Peaks in der DSC-Kurve angezeigt, der der Freisetzung von Wärme entspricht, wenn die Probe oxidiert. Die Zeit, zu der der exotherme Peak auftritt, wird als Oxidationsinduktionszeit (OIT) bezeichnet und ist ein Maß für die Widerstandsfähigkeit der Probe gegen Oxidation. Die Methode ist in Abb. 1 dargestellt.
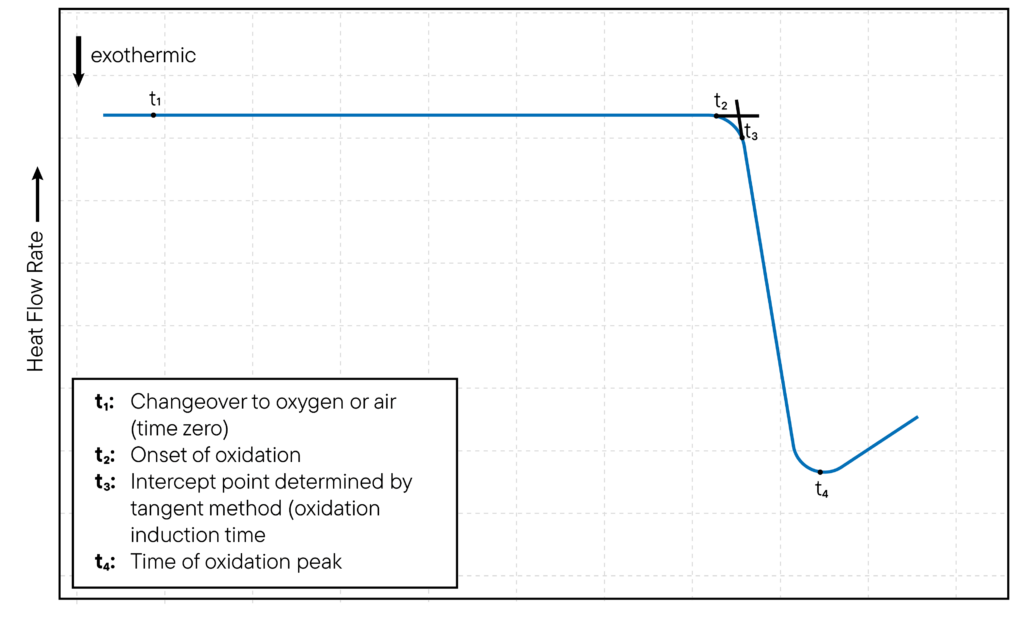
Bei nicht-isothermen Oxidationsstudien wird die Temperatur der DSC-Zelle mit einer konstanten Rate erhöht und die Oxidation der Probe als Funktion der Temperatur überwacht.
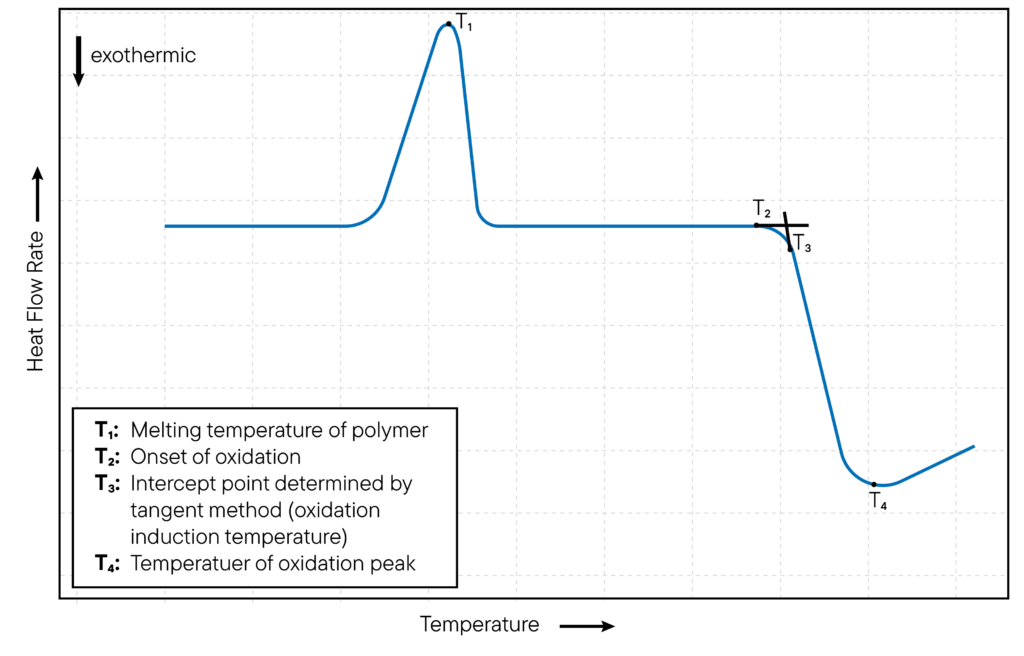
Das DSC-Gerät erkennt einen exothermen Peak in der DSC-Kurve, wenn eine Probe oxidiert und Wärme freigesetzt wird. Die Temperatur, bei der der Peak auftritt, wird als Oxidationsanfangstemperatur (OOT) bezeichnet.
Die Methode ist in Abb. 2 dargestellt. Die OOT ist ein Maß für die thermische Stabilität der Probe und wird zur Bewertung der oxidativen Stabilität von Materialien verwendet.
Zusammenfassend lässt sich sagen, dass durch die Messung der Oxidationsinduktionszeit (OIT) oder der Oxidationsbeginntemperatur (OOT) bei verschiedenen Temperaturen die Aktivierungsenergie für die Oxidation bestimmt werden kann, was Aufschluss über die thermische Stabilität der Probe gibt.
DSC kann auch verwendet werden, um die Auswirkungen von Antioxidantien und anderen Zusatzstoffen auf die Oxidationsstabilität von Proben zu bewerten, was für deren Qualität und Haltbarkeit wichtig ist.
DSC kann auch zur Bestimmung der Aktivierungsenergie für die Oxidation verwendet werden, die ein Maß für die zur Einleitung des Oxidationsprozesses erforderliche Energie ist.
Die Aktivierungsenergie kann anhand der Arrhenius-Gleichung berechnet werden, die die Geschwindigkeit einer chemischen Reaktion mit der Temperatur, bei der sie stattfindet, in Beziehung setzt. Die Aktivierungsenergie für die Oxidation kann durch Messung der Oxidationsinduktionszeit (OIT) oder der Oxidationsbeginntemperatur (OOT) bei verschiedenen Temperaturen und Aufzeichnung der Daten in einem Arrhenius-Diagramm bestimmt werden.
Die Steigung der resultierenden Linie wird zur Berechnung der Aktivierungsenergie für die Oxidation verwendet. Die DSC-Kurve kann analysiert werden, um verschiedene Parameter im Zusammenhang mit der Oxidation zu bestimmen, z. B. die Anfangstemperatur, die Spitzentemperatur und die Oxidationswärme.
Sowohl OIT als auch OOT sind wichtige Parameter für die Bewertung der Oxidationsstabilität von Materialien, und die Wirksamkeit von Antioxidantien kann insbesondere bei Polymeren verglichen werden.
Eine längere OIT oder eine höhere OOT weist auf eine größere oxidative Stabilität und Widerstandsfähigkeit gegenüber dem Abbau hin. Zu den Faktoren, die sich auf die Genauigkeit der DSC-Messungen für die Oxidation auswirken können, gehören die Probenvorbereitung, die Instrumentierung und die Versuchsbedingungen, wie z. B. die Heizrate und die Atmosphäre.
Die thermische Analyse kann zur Untersuchung der Oxidation von Metallen in einer sauerstoffhaltigen Atmosphäre eingesetzt werden, in der sich ein Metalloxid bildet und die temperatur- oder zeitabhängige Massenzunahme mit Techniken wie der TGA beobachtet werden kann.
Zersetzung während der Oxidation
Referenzen:
- Stephen M. Hsua and Chun-I Chenb, A chemical kinetics model to predict diesel engine performance.Part II. Bench-test procedures: Tribology Letters, Vol. 14, No. 2, February 2003.
- B. Wunderlich, Thermal Analysis of Polymeric Materials. Berlin, Heidelberg: Springer-Verlag Berlin Heidelberg, 2005.
- G. W. Ehrenstein, G. Riedel und P. Trawiel, Thermal analysis of plastics: Theory and practice. Munich: Hanser, 2004.
- Plastics – Differential Scanning Calorimetry (DSC), ISO 11357-6, 2008.
- Mahbuba Islam, Anna Kaczmarek, and Jolanta Tomaszewska-Gras, Differential scanning calorimetry as a tool to assess the oxidation state of cold-pressed oils during shelf-life: Journal of Food Measurement and Characterization (2023) 17:6639–6651.