목차
흡열 반응과 발열 반응의 차이점은 무엇인가요?
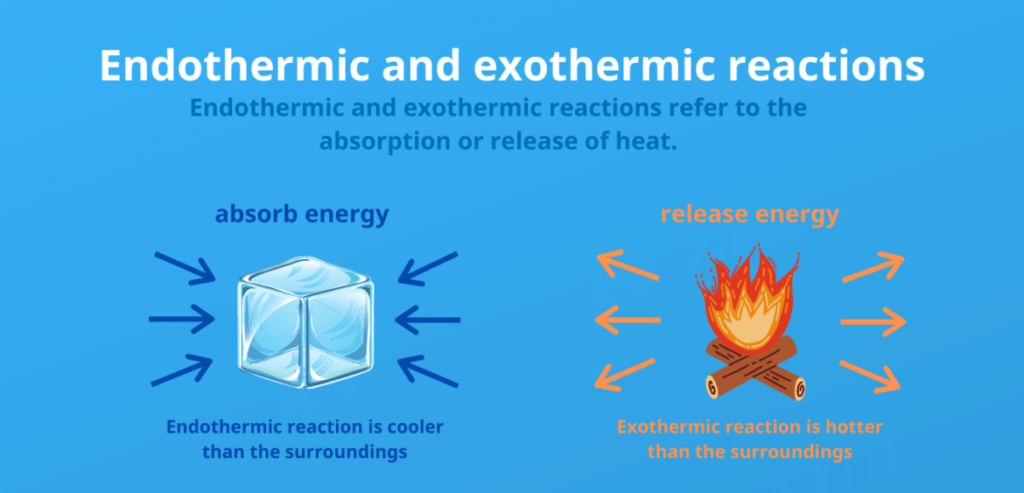
발열 반응과 흡열 반응의 주요 차이점은 주변 환경과의 열 교환에 있습니다:
- 흡열 반응은 주변에서 열의 형태로 에너지를 흡수 를 주변으로부터 열의 형태로 흡수하여 주변을 더 차갑게 만듭니다.
즉, 생성물이 반응물보다 더 많은 에너지를 가지며 반응에는 열이 필요하므로 엔탈피(ΔH)가 양의 변화로 이어집니다. - 발열 반응은 열의 형태로 에너지를 방출 를 열의 형태로 주변으로 방출하여 주변을 더 따뜻하게 만듭니다.
이 경우 생성물은 반응물보다 에너지가 적고 반응은 열을 방출하여 엔탈피(ΔH)가 음의 변화로 이어집니다.
발열 반응 또는 흡열 반응을 식별하는 방법은 무엇인가요?
발열 반응을 인식하는 방법에는 두 가지가 있습니다:
- 온도 변화:
- 발열 반응에서는 에너지가 방출되어 반응 혼합물의 온도가 상승합니다. 반대로 흡열 반응에서는 에너지가 흡수되어 온도가 낮아집니다. 온도계를 반응 혼합물에 넣으면 온도 변화를 관찰할 수 있습니다.
- 엔탈피 변화:
- 엔탈피(ΔH)의 변화는 생성물의 에너지와 반응물의 에너지 사이의 차이입니다. ΔH가 음수이면 반응물을 분해하는 데 사용되는 에너지보다 생성물이 형성될 때 더 많은 에너지가 방출되므로 발열 화학 반응을 나타냅니다. ΔH가 양수이면 반응물을 분해하는 데 사용된 에너지보다 생성물이 형성될 때 방출되는 에너지가 적기 때문에 흡열 화학 반응을 나타냅니다.
발열 반응과 흡열 반응은 환경에 미치는 영향이 다릅니다:
발열 반응은 환경으로 열을 방출하여 환경에 긍정적인 영향을 미칠 수도 있고 부정적인 영향을 미칠 수도 있습니다. 발열 반응은 호흡, 연소, 에너지 생산과 같은 과정에 관여합니다. 하지만 발열 반응은 대기 및 수질 오염과 같은 환경 문제에도 기여할 수 있습니다.
발열 반응의 추가 예시:
- 목재 또는 석탄 연소:
- 나무나 석탄이 연소하면 열이 방출되어 발열 반응이 일어납니다. 이러한 반응은 히터, 용광로 및 에너지 생산을 위한 엔진에 사용됩니다.
- 금속의 산화:
- 철이 녹을 형성하는 것처럼 금속이 산소와 반응하면 열이 방출되는 발열 반응이 일어납니다.
- 화학 폭발물:
- 화학 폭발물의 폭발은 열과 압력의 형태로 대량의 에너지를 방출하는 발열 반응입니다.
흡열 반응은 주변에서 열을 흡수합니다. 광합성이나 요리와 같은 과정에는 필수적이지만 일반적으로 발열 반응에 비해 환경에 미치는 직접적인 영향은 적습니다.
흡열 반응의 추가 예시:
- 광합성:
- 광합성 과정에서 식물은 공기 중의 이산화탄소를 흡수하고 빛 에너지를 사용하여 당과 산소로 전환합니다. 이것은 빛의 형태로 에너지가 흡수되는 흡열 반응입니다.
- 끓는 물:
- 물을 가열하여 끓이는 것은 흡열 반응입니다. 끓는 과정에서 열 형태의 에너지가 공급되어 물 입자를 증기로 변환합니다.
- 물에 소금 녹이기:
- 소금이 물에 녹으면 소금 분자는 주변에서 열을 흡수하여 결정을 분해하고 용해된 형태로 분산됩니다.