이 연구에서는 질산칼슘 사수화물 – Ca(NO3)2.
4H2O의측정 결과를 발표하고 논의합니다.
이 소금은 저렴하고 매우 효과적이기 때문에 이미 열 저장 및 열 전달 재료로 널리 사용되고 있습니다.
샘플은 무게 변화와 DSC 신호를 동시에 모니터링하는 Linseis STA PT 1000 기기를 사용하여 분석했습니다.
상 전이의 엔탈피와 열 용량은 DSC 신호에서 확인할 수 있습니다.
샘플을 밀폐된 알루미늄 도가니에서 10K/min의 가열 속도로 180°C까지 가열한 후 3시간 동안 등온을 유지했습니다.
그런 다음 10K/min의 가열 속도로 600°C까지 가열했습니다.
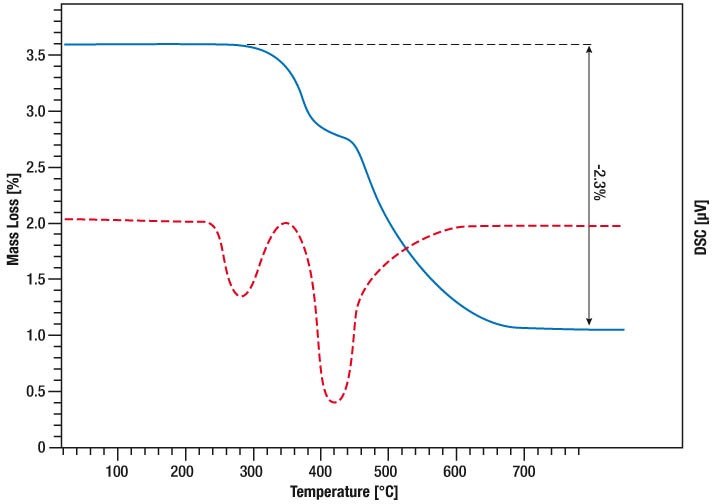
파란색 곡선은 질량 손실을, 빨간색 곡선은 DSC 신호를 나타냅니다.
DSC 신호의 첫 번째 피크는 시료의 용융으로 인해 발생합니다.
용융 피크의 시작은 46°C입니다.
시료가 완전히 녹은 후 141°C에서 시작되는 두 번째 흡열 피크가 발생합니다.
TG 신호는 이 온도 범위에서 32%의 중량 감소를 보여줍니다.
질산칼슘 사수화물의 결정화 물이 분리되어 고체 무수염이 형성됩니다.
180°C에서 등온 유지 시간 동안 샘플은 더 이상의 변화를 겪지 않으므로 이 온도는 소금을 건조하고 무수염을 얻는 데 이상적입니다.
다시 541°C로 가열하면 흡열 피크가 발생합니다.
무수염이 녹습니다.
그러나 TG 신호는 무게 감소를 보여줍니다.
이것은 소금이 녹는 동안 분해된다는 것을 나타냅니다.
따라서 융합 엔탈피와 용융된 무수염의 열용량은 직접 측정할 수 없습니다.
그러나 이는 소금 혼합물의 추가 TG-DSC 측정을 통해 달성할 수 있습니다.
질산 칼슘은 리튬, 나트륨 또는 질산 칼륨과 서로 다른 몰 비율로 혼합해야 합니다.
융합 엔탈피는 혼합물의 DSC 용융 피크로부터 결정할 수 있습니다.
그런 다음 순수한 질산 칼슘의 융합 엔탈피는 질산 칼슘에 대한 몰 백분율 100%로 외삽하여 간단히 계산할 수 있습니다.
용융된 무수 질산칼슘의 열용량을 측정하는 데에도 동일한 방법이 사용됩니다.


