Description
En bref
Différence entre la vapeur d’eau et l’humidité relative dans l’analyse thermique
Lorsque l’eau est chauffée à son point d’ébullition ou au-delà, elle passe de l’état liquide à l’état gazeux. Elle se présente alors sous forme de vapeur (d’eau). Lorsque cette vapeur est introduite dans une chambre de réaction ou un appareil, on parle d’application de vapeur d’eau.
En revanche, tout gaz peut transporter et contenir une certaine quantité d’eau à une température donnée. C’est ce que l’on appelle l’humidité. Si l’on prend l’exemple de l’air, on constate que même en dessous du point d’ébullition de l’eau, l’air contient toujours une certaine quantité d’eau, appelée taux d’humidité ou humidité relative.
Contrairement à l’humidité relative, au-dessus du point d’ébullition dépendant de la pression, qui est de 100°C au niveau de la mer, l’eau n’est présente que dans sa phase gazeuse, sous forme de vapeur d’eau. En mélangeant de la vapeur d’eau, produite dans un générateur de vapeur d’eau, avec un gaz porteur comme l’air, l’azote ou l’hélium, il est possible de régler de manière variable la concentration (en % vol., % poids ou ppm) de la vapeur d’eau dans le gaz de mesure pour les analyseurs.
En outre, l’atmosphère gazeuse dans l’appareil peut être statique ou dynamique, selon l’application. Les études typiques pour les atmosphères de vapeur d’eau dynamiques comprennent le chauffage isotherme d’un échantillon et le dosage ultérieur d’une concentration définie de vapeur d’eau pour initier une réaction. Il peut s’agir, par exemple, de mesures d’adsorption, de désorption, de réduction, d’oxydation ou de conversion.
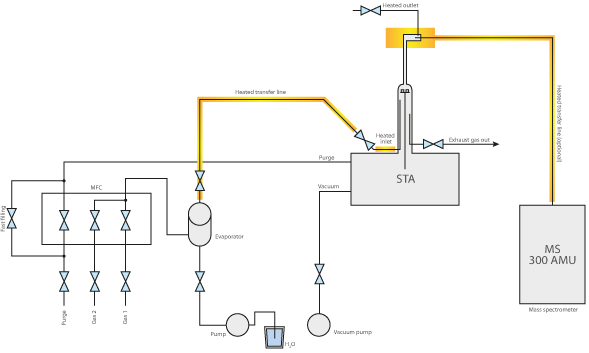
Pour l’analyse thermique, les générateurs de vapeur d’eau sont généralement utilisés en combinaison avec des thermobalances telles que TGA et STA (dans le domaine des hautes pressions) ainsi que des dilatomètres.

Mesures en fonction de la pression sous atmosphère de vapeur d'eau
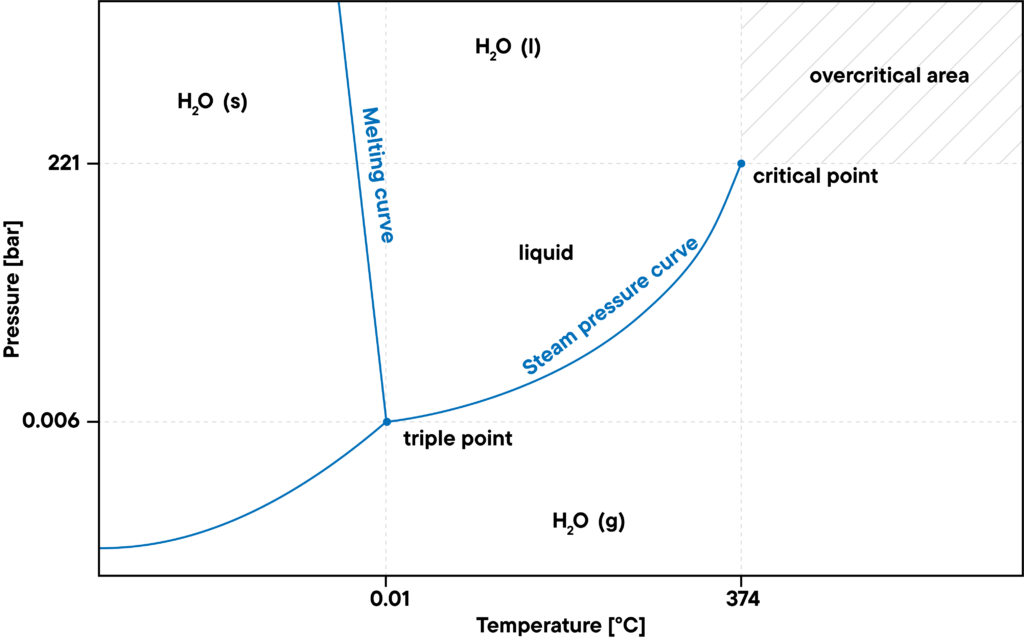
D’autre part, le niveau de pression maximal de l’eau gazeuse est défini par la courbe de saturation de pression de vapeur. Si la pression devient trop élevée, l’eau se condense. A des températures ou des pressions plus élevées, au-dessus du point critique, la densité de l’eau liquide est aussi grande que celle de l’eau gazeuse, de sorte qu’elle ne peut plus se condenser. C’est ce qu’on appelle l’état supercritique, par exemple la vapeur d’eau surchauffée.
Service d'assistance téléphonique
+49 (0) 9287/880 0
Notre service est disponible du lundi au
jeudi de 8h à 16h
et vendredi de 8h à 12h.
Nous sommes là pour vous !
Votre industrie
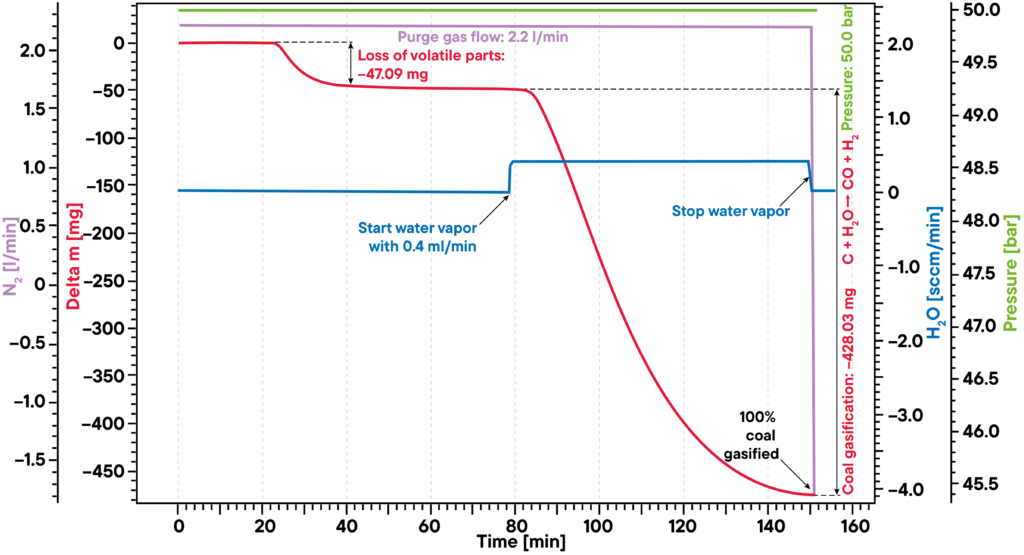
Les essais de gazéification du charbon et de la biomasse sont un exemple typique d’application de la vapeur d’eau à des températures et des pressions élevées. L’exemple donné montre une expérience typique de gazéification du charbon de bois. L’échantillon de charbon a été chauffé sous atmosphère d’azote à une pression de 50 bars jusqu’à un plateau isotherme (TGA haute pression – thermobalance). Le signal de masse indique la perte de composants volatils entre 20 et 40 minutes. Après l’ajout de vapeur d’eau, le charbon a été gazéifié et presque entièrement consommé après 150 minutes, produisant H2, CO, CH3OH et d’autres gaz réactifs utiles, comme le montre la courbe de perte de masse rouge. L’ensemble du processus peut être décrit comme suit : Le carbone réagit avec la vapeur d’eau pour former un mélange de monoxyde de carbone et d’hydrogène. Le monoxyde de carbone ainsi produit peut réagir avec une deuxième molécule d’eau pour former du dioxyde de carbone et de l’hydrogène supplémentaire et, finalement, l’hydrogène produit peut former du méthane et d’autres hydrocarbures à partir du monoxyde de carbone.
Bien informé


