En este estudio, se presentan los resultados de las mediciones TG-DSC del nitrato de calcio tetrahidratado – Ca(NO3)2.
4H2O-.
Esta sal ya se utiliza ampliamente como material para el almacenamiento y la transferencia de calor, ya que es barata y extremadamente eficaz.
La muestra se analizó con un instrumento Linseis STA PT 1000, que controla simultáneamente el cambio de peso y la señal DSC.
La entalpía de las transiciones de fase y la capacidad calorífica pueden determinarse a partir de la señal DSC.
La muestra se calentó en crisoles de aluminio cerrados hasta 180 °C a una velocidad de calentamiento de 10 K/min y se mantuvo isotérmica durante 3 horas.
Después se calentó a 600 °C a una velocidad de calentamiento de 10 K/min.
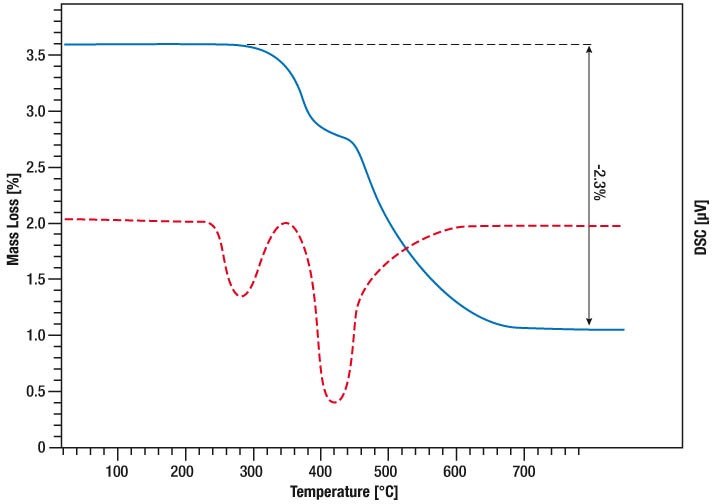
La curva azul muestra la pérdida de masa y la curva roja la señal DSC.
El primer pico de la señal DSC se debe a la fusión de la muestra.
El inicio del pico de fusión se sitúa a 46 °C.
Tras la fusión completa de la muestra, se produce un segundo pico endotérmico con inicio a 141 °C.
La señal TG muestra una pérdida de peso del 32 % en este intervalo de temperatura.
El agua de cristalización del nitrato cálcico tetrahidratado se desprende y se forma una sal sólida anhidra.
Durante el tiempo de mantenimiento isotérmico a 180 °C, la muestra no sufre más cambios, lo que significa que esta temperatura es ideal para secar la sal y obtener la sal anhidra.
Cuando se calienta de nuevo a 541 °C, se produce un pico endotérmico.
La sal anhidra se funde.
Sin embargo, la señal TG muestra una pérdida de peso.
Esto indica que la sal se descompone durante la fusión.
Por tanto, la entalpía de fusión y la capacidad calorífica de la sal anhidra fundida no pueden medirse directamente.
Sin embargo, esto puede conseguirse mediante nuevas mediciones TG-DSC de mezclas de sales.
El nitrato de calcio debe mezclarse con nitrato de litio, sodio o potasio en diferentes porcentajes molares.
Las entalpías de fusión pueden determinarse a partir de los picos de fusión DSC de las mezclas.
A continuación, la entalpía de fusión del nitrato de calcio puro puede calcularse simplemente por extrapolación a un porcentaje molar del 100 % en relación con el nitrato de calcio.
El mismo método se utiliza para medir la capacidad calorífica del nitrato cálcico anhidro fundido.


