In dieser Studie werden Ergebnisse von TG-DSC-Messungen an Calciumnitrat-Tetrahydrat – Ca(NO3)2 . 4H2O – präsentiert und diskutiert. Dieses Salz wird bereits weit verbreitet als Material zur Wärmespeicherung und Wärmeübertragung eingesetzt, da es kostengünstig und äußerst effektiv ist.
Die Probe wurde mit einem Linseis STA PT 1000 Instrument untersucht, das gleichzeitig die Gewichtsveränderung und das DSC-Signal überwacht. Aus dem DSC-Signal können die Enthalpie der Phasenübergänge und die Wärmekapazität ermittelt werden.
Die Probe wurde in geschlossenen Aluminiumtiegel bis auf 180 °C mit einer Heizrate von 10 K/min erwärmt und für 3 Stunden isotherm gehalten. Danach wurde sie auf 600 °C mit einer Heizrate von 10 K/min erhitzt.
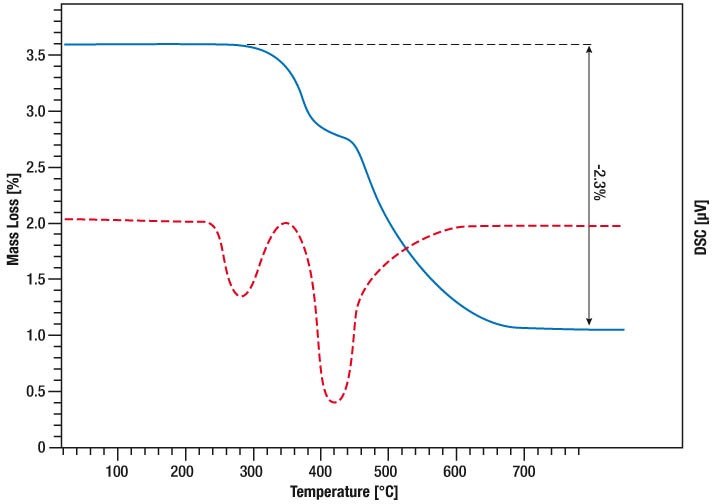
Die blaue Kurve zeigt den Massenverlust und die rote Kurve das DSC-Signal. Der erste Peak im DSC-Signal entsteht durch das Schmelzen der Probe. Der Beginn des Schmelzpeak liegt bei 46 °C.
Nach dem vollständigen Schmelzen der Probe entsteht ein zweiter endothermer Peak mit einem Onset bei 141 °C. Das TG-Signal zeigt einen Gewichtsverlust von 32 % in diesem Temperaturbereich. Dabei wird das Kristallwasser des Calciumnitrat-Tetrahydrats abgespalten und es bildet sich festes wasserfreies Salz.
Während der isothermen Haltezeit bei 180 °C unterliegt die Probe keinen weiteren Veränderungen, was bedeutet, dass diese Temperatur ideal ist, um das Salz zu trocknen und das wasserfreie Salz zu erhalten.
Bei erneuter Erhitzung auf 541 °C entsteht ein endothermer Peak. Das wasserfreie Salz schmilzt. Allerdings zeigt das TG-Signal einen Gewichtsverlust. Dies deutet darauf hin, dass das Salz beim Schmelzen zerfällt. Daher können die Schmelzenthalpie und die Wärmekapazität des geschmolzenen wasserfreien Salzes nicht direkt gemessen werden.
Dies kann jedoch durch weitere TG-DSC-Messungen von Salzmischungen erreicht werden. Das Calciumnitrat muss mit Lithium-, Natrium- oder Kaliumnitrat in unterschiedlichen Molprozenten gemischt werden. Aus den DSC-Schmelzpeaks der Mischungen können die Schmelzenthalpien ermittelt werden. Die Schmelzenthalpie des reinen Calciumnitrats kann dann einfach durch Extrapolation auf einen Molprozentsatz von 100 % bezogen auf das Calciumnitrat berechnet werden.
Das gleiche Verfahren wird verwendet, um die Wärmekapazität des geschmolzenen wasserfreien Calciumnitrats zu messen.


